6)「製造販売承認書の点検」に関する進捗状況
当社製造販売品目を対象とした製造販売承認書の記載内容と製造実態の整合性に係る点検状況は以下の通りです。
調査結果受領済み(254/254件:100%)
2023年3月31日時点



第一三共エスファ株式会社(本社:東京都中央区、以下「当社」)は、後発医薬品の品質にかかる問題に対して、品質管理を強化していきます。患者さん、医療関係者さま、その他すべての関係する方に、より安心して当社の製品をご使用いただくために、法令遵守の責任体制と製造委託先管理に関する事項について情報を開示します。
社長を最上位責任者として、責任役員、製造販売業の三役が各々の責任を果たし、品質確保に努めます。
| 開発 | 薬剤 | 品質保証 | 安全管理 | 広告 | コンプライアンス | 販売 | ||
|---|---|---|---|---|---|---|---|---|
| 代表取締役社長 | 新堰 毅 | ○ | ○ | ○ | ○ | ○ | ○ | ○ |
| 取締役 経営本部長 | 名取 宏祐 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 取締役 営業本部長 | 赤坂 大介 | ○ | ○ | |||||
| 取締役 経営本部 信頼性保証部長 |
竹野下 治洋 | ○ | ○ | ○ | ○ | ○ | ○ | |

| 医薬品等総括製造販売責任者 | 神庭 正晴(薬剤師) 経営副本部長 |
|---|---|
| 医薬品等安全管理責任者 | 福田 文康(薬剤師) 信頼性保証部 安全性情報管理グループ長 |
| 医薬品等品質保証責任者 | 豊田 智則(薬剤師) 信頼性保証部 品質保証グループ長 |
1)製造業者等との取り決め
製造販売業者として、原薬及び製剤の製造業者等における製造管理及び品質管理の適正かつ円滑な実施を確保するために、製品の製造業者等と製造方法、試験検査方法等に関する技術的条件や弊社による製造業者への定期的な確認(GMP監査)等について取り決めをしております。
(弊社が管理する製造業者)
全製造所数 : 227
所在地別分類: 国内114、海外113
製造所区分 : 製剤59 原薬・中間体132 その他36
2)製造業者へのGMP監査
製造業者等との取り決めに基づき、原則として初回の製造所監査は実地で行い、以降の定期的な監査はリスクに応じて1年~5年の周期で実地または書面の確認による監査を実施しています。
・GMP監査の実施状況【2022年度実績】
| 海外 | 国内 | ||
|---|---|---|---|
| 監査実施件数 | 対象施設数 | 監査実施件数 | 対象施設数 |
| 12 | 136 | 38 | 120 |
※対象施設は原薬製造所、製剤製造所、試験施設、保管所等
3)逸脱処理
製造所から定められた手順、管理基準あるいは試験規格等から乖離してしまったという「逸脱」の連絡を受けた場合に、品質への影響を確認して、出荷可能かどうかを評価し、再発防止等の必要な措置を取っています。
・逸脱処理件数【2022年度実績】 101件
4)変更管理
医薬品の品質に影響を与える可能性のある全ての変更事項を対象として、事前に品質への影響レベルの評価を行い、変更完了まで追跡管理を行っています。
・変更管理起案件数【2022年度実績】 221件
5)品質情報の処理
医療機関等から医薬品に係る品質等に関する情報(品質情報)を得た時には、品質、有効性及び安全性に与える影響並びに人の健康に与える影響を適正に評価しています。製造に起因する不具合であることが判明した場合には、原因を究明し、再発防止策を取っています。
・医療機関等からの不具合などのお申し出件数【2022年度実績】 218件
6)「製造販売承認書の点検」に関する進捗状況
当社製造販売品目を対象とした製造販売承認書の記載内容と製造実態の整合性に係る点検状況は以下の通りです。
調査結果受領済み(254/254件:100%)
2023年3月31日時点
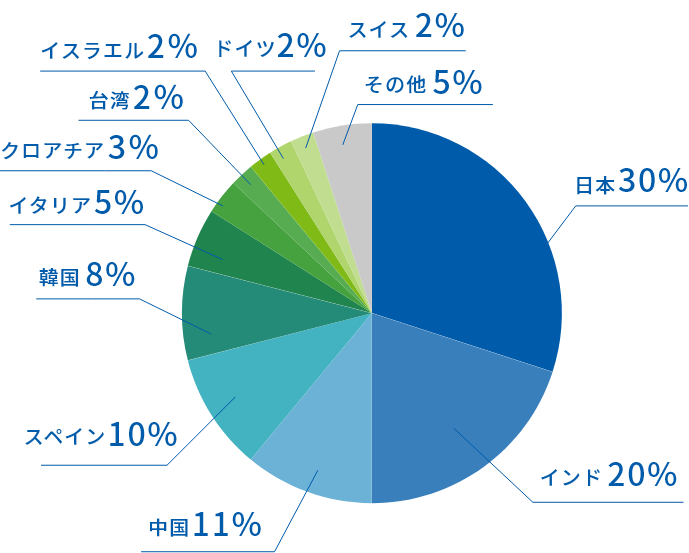
原薬の調達国の状況は以下の通りで、338ある原薬の調達先の上位は、日本(30%)、インド(20%)、中国(11%)となっています。
| 原薬数 | 338 | |
|---|---|---|
| 日本 | 100 | 30% |
| インド | 69 | 20% |
| 中国 | 38 | 11% |
| スペイン | 33 | 10% |
| 韓国 | 26 | 8% |
| イタリア | 18 | 5% |
| クロアチア | 11 | 3% |
| 台湾 | 8 | 2% |
| イスラエル | 7 | 2% |
| ドイツ | 6 | 2% |
| スイス | 6 | 2% |
| その他 | 15 | 5% |